Un equipo clínico multidisciplinar con participación del Instituto de Bioingeniería de la Universidad Miguel Hernández de Elche (UMH) ha desarrollado un nuevo método para administrar terapias celulares en pacientes críticos conectados a sistemas de oxigenación por membrana extracorpórea.
 Este avance, liderado por el catedrático de la UMH Bernat Soria, ha sido publicado en la revista Stem Cell Research & Therapy del Grupo Springer Nature. Los investigadores han decidido no patentar la invención para facilitar su aplicación clínica una vez superados todos los ensayos previos.
Este avance, liderado por el catedrático de la UMH Bernat Soria, ha sido publicado en la revista Stem Cell Research & Therapy del Grupo Springer Nature. Los investigadores han decidido no patentar la invención para facilitar su aplicación clínica una vez superados todos los ensayos previos.
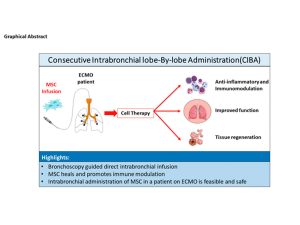
El nuevo enfoque, bautizado como método CIBA (Consecutive Intrabronchial Administration, o Administración Consecutiva Intrabronquial), permite aplicar tratamientos basados en células madre directamente en los pulmones de pacientes conectados a oxigenación por membrana extracorpórea, un tipo de soporte vital utilizado en situaciones de fallo respiratorio extremo.
Hasta ahora, una de las principales limitaciones para aplicar terapias avanzadas en estos pacientes era la incompatibilidad entre las vías de administración convencionales (como la intravenosa) y el funcionamiento de estos sistemas, ya que las células podían obstruir las membranas encargadas del intercambio de gases. El método CIBA supera esta barrera técnica mediante una administración intrabronquial controlada y fraccionada que permite depositar las células terapéuticas en el espacio alveolar sin comprometer el soporte vital.
“Lo que hemos conseguido —explica Bernat Soria— es abrir una nueva puerta para tratar los fallos respiratorios más graves. Cuando un paciente necesita una máquina para respirar por él, las terapias celulares no se podían administrar por las vías habituales, porque las células podían atascar el sistema. Nuestro método permite entregarlas directamente en el pulmón, sin poner en riesgo al paciente. Es como regar con cuidado una planta muy delicada: poco a poco y justo donde lo necesita.”
El nuevo método permite administrar células madre mesenquimales directamente en los bronquios. Estas células, que aún no están completamente especializadas y pueden diferenciarse en varios tipos celulares, pueden obtenerse de médula ósea, cordón umbilical, tejido adiposo o pulpa dental. Una vez administradas, tienen la capacidad de migrar hacia los tejidos dañados, reducir la inflamación y favorecer la reparación pulmonar.
Según los autores, esta estrategia ha demostrado ser factible y segura en el contexto clínico descrito y podría abrir una nueva vía de tratamiento para pacientes en estado crítico debido a enfermedades pulmonares de origen inflamatorio, inmunológico o infeccioso.
“Los pacientes con enfermedades pulmonares graves que requieren oxigenación por membrana extracorpórea suelen tener un pronóstico muy limitado y pocas opciones terapéuticas”, apunta el catedrático de la UMH. Como se indica en el estudio, aunque las células madre mesenquimales han mostrado efectos beneficiosos en enfermedades inflamatorias, inmunológicas e infecciosas, su uso en estos casos estaba impedido por la dificultad de administrarlas sin interferir con el soporte vital. “El nuevo método CIBA resuelve por primera vez este problema”, afirma el investigador.
El método propuesto por el equipo de Bernat Soria se ha desarrollado dentro del ensayo clínico DECODE (ICI21/00016-Combinatorial Cell Therapy in High Mortality Risk Patients), financiado por el Instituto de Salud Carlos III, y representa un paso clave para extender el uso de terapias avanzadas —celulares y génicas— a pacientes en estado crítico. El equipo investigador ha decidido no patentar la técnica, publicándola en acceso abierto para facilitar su aplicación inmediata en otros centros hospitalarios. “Las terapias avanzadas ya son lo suficientemente caras. Esta innovación tiene que llegar a los pacientes a coste cero”, ha declarado el catedrático de la UMH Bernat Soria.
El nuevo método se aplicó por primera vez en un niño de dos años con enfermedad pulmonar intersticial grave, sin posibilidad de trasplante pulmonar y con una historia previa de tratamiento exitoso contra un tumor cerebral. A pesar de múltiples terapias inmunosupresoras y de más de tres meses conectado a oxigenación por membrana extracorpórea, su estado pulmonar no mejoraba y no quedaban opciones terapéuticas disponibles.
Ante esta situación crítica, el equipo médico solicitó a la Agencia Española del Medicamento y Productos Sanitarios (AEMPS) administrar una dosis única de células madre mesenquimales utilizando el método CIBA. La intervención se llevó a cabo sin complicaciones, el paciente la toleró bien y fue extubado a las 72 horas. Sin embargo, con el paso de las semanas su estado respiratorio volvió a empeorar. Tras 127 días de soporte vital, y en consenso con la familia, se procedió a la retirada del soporte vital.
“El nuevo método CIBA no pudo curar la enfermedad pulmonar subyacente”, explica el profesor de la UMH, “pero demuestra que es posible aplicar terapias celulares en pacientes críticos con oxigenación extracorpórea, algo que hasta ahora no se había logrado con seguridad. Es un primer paso para abrir nuevas opciones donde antes no las había”. En el trabajo publicado se proponen una dosis más alta y la repetición de las dosis si se considera necesario.
En el estudio han participado 28 profesionales clínicos de cuatro instituciones del sistema nacional de salud y del ámbito universitario: el Hospital 12 de Octubre de Madrid, el Banc de Sang i Teixits de Catalunya, el Instituto de Bioingeniería de la UMH y el Instituto de Investigación Sanitaria y Biomédica de Alicante (ISABIAL). Esta colaboración, que Soria describe como “ejemplo de coordinación entre hospitales, biobancos e investigación académica”, permite avanzar en la traslación clínica de las terapias celulares en escenarios de alta complejidad médica.
Acceso al artículo:
Nerea Dominguez-Pinilla et al “Consecutive IntraBronchial Administration of Wharton’s Jelly-Derived Mesenchymal Stromal Cells in ECMO-Supported Pediatric Patients with End-Stage Interstitial Lung Disease: A Safety and Feasibility Study (CIBA Method). Stem Cell Research & Therapy. 2025. doi: 10.1186/s13287-025-04289-3